我国医疗器械行业的主管部门为国家发展和改革委员会、国家食品药品监督管理总局、国家卫生和计划生育委员会。其中,国家发展和改革委员会负责组织实施产业政策,研究拟定医疗器械行业发展规划,指导行业结构调整和实施行业管理;国家食品药品监督管理总局负责对医疗器械企业的研制、生产、流通和使用进行行政监督和技术管理;国家卫生和计划生育委员会负责制定医疗机构和医疗服务全行业管理办法并监督实施。
2、行业自律组织
我国医疗器械行业的自律机构为中国医疗器械行业协会,主要负责开展有关行业发展问题的调查研究,向政府有关部门提供政策和立法等方面的意见和建议,组织制定并监督执行行业政策,参与国家标准、行业标准、质量规范的制定、修改、宣传和推广,开展行业资质管理工作等。协会在遵守国家政策法规的基础上,维护会员单位的合法权益,促进中国医疗器械行业健康发展。
3、行业监管体制
我国医疗器械行业实行产品管理和市场准入管理,既监督产品,又监督生产、经营企业。
(1)产品管理
1)医疗器械分类管理
我国对医疗器械实行分类管理,按风险程度由低到高,依次分为第一类(Ⅰ类)、第二类(Ⅱ类)和第三类(Ⅲ类)。第一类是风险程度低,实行常规管理足以保证其安全、有效的医疗器械;第二类是具有中度风险,需要严格控制管理以保证其安全、有效的医疗器械;第三类是具有较高风险,需要采取特别措施严格控制管理以保证其安全、有效的医疗器械。
2)医疗器械产品注册与备案管理
我国对医疗器械实行产品注册与备案管理制度,第一类医疗器械产品备案管理,第二类、第三类医疗器械实行产品注册管理。第一类医疗器械产品备案,由备案人向所在地设区的市级食品药品监督管理部门提交备案资料;第二类医疗器械产品注册,由注册人向所在地省、自治区、直辖市食品药品监督管理部门提交注册申请资料,食品药品监督管理部门审查批准后颁发医疗器械注册证书。第三类医疗器械产品注册,由注册人向国家食品药品监督管理部门提交注册申请资料,食品药品监督管理部门审查批准后颁发医疗器械注册证。
(2)市场准入管理
1)医疗器械生产
企业生产许可与备案管理我国对医疗器械生产企业实行生产许可与备案管理制度,第一类医疗器械生产企业实行备案管理,第二类、第三类医疗器械生产企业实行生产许可管理。开办第一类医疗器械生产企业的,应当向所在地设区的市级食品药品监督管理部门提交备案资料,办理生产备案;开办第二类、第三类医疗器械生产企业的,应当向所在地省、自治区、直辖市食品药品监督管理部门申请生产许可,食品药品监督管理部门审查批准后颁发医疗器械生产许可证。
参考观研天下发布《2018年中国医疗器械行业分析报告-市场运营态势与发展前景研究》
2)医疗器械经营企业许可与备案管理
我国对医疗器械经营企业实行许可与备案管理制度,经营第一类医疗器械不需要许可和备案,经营第二类医疗器械实行备案管理,经营第三类医疗器械实行许可管理。从事第二类医疗器械经营的,应当向所在地设区的市级食品药品监督管理部门备案;从事第三类医疗器械经营的,应当向所在地设区的市级食品药品监督管理部门提出申请,食品药品监督管理部门审查批准后颁发医疗器械经营许可证。
4、行业主要法律法规

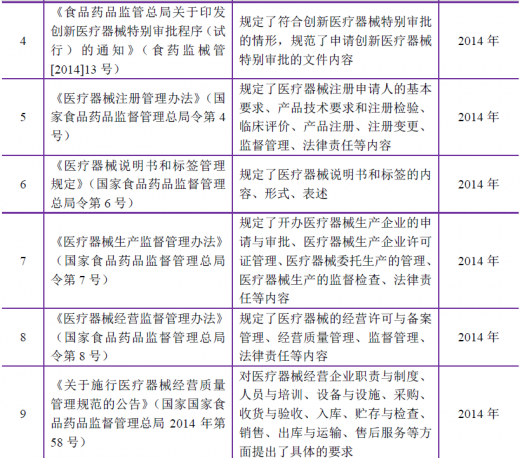
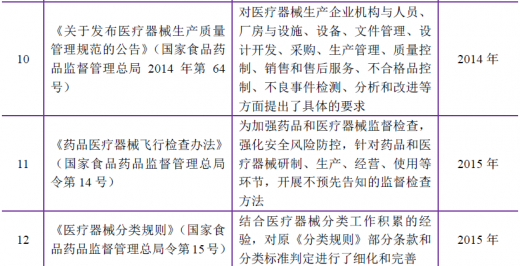
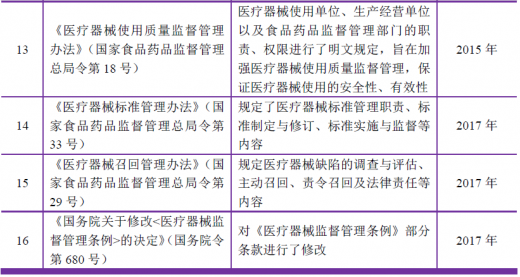
医疗器械行业属于国家重点鼓励和发展的行业。近年来,国务院、政府主管部门出台了一系列振兴医疗器械行业的产业政策,主要如下:
(1)《产业技术创新能力发展规划(2016-2020年)》
2016年10月21日,工业和信息化部印发了《产业技术创新能力发展规划(2016-2020年)》,提出在高性能医疗器械方面,加快医疗设备数字化、网络化和智能化发展,加强数字化影像设备等高性能诊疗设备,全降解血管支架等高值医用耗材,可穿戴、远程诊疗等移动医疗产品,诱导多能干细胞等新技术开发,提高医疗器械的创新能力和产业化水平。
(2)《“健康中国”2030规划纲要》
2016年10月25日,中共中央、国务院印发了《“健康中国2030”规划纲要》,提出要加快医疗器械转型升级,提高具有自主知识产权的医学诊疗设备、医用材料的国际竞争力,到2030年,药品、医疗器材质量标准全面与国际接轨。
(3)《“十三五”国家战略性新兴产业发展规划》
2016年11月29日,国务院印发了《“十三五”国家战略性新兴产业发展规划》,提出加快组织器官修复和替代材料及植介入医疗器械产品创新和产业化。
(4)《战略性新兴产业重点产品和服务指导目录》(2016版)
2017年1月25日,国家发改委公布了《战略性新兴产业重点产品和服务指导目录》(2016版),将“植介入生物医用材料及服务”列为战略性新兴产业重点产品和服务。
(5)《“十三五”卫生与健康科技创新专项规划》
2017年6月7日,科技部、卫计委、体育总局、国家食药总局、国家中医药管理局、中央军委后勤保障部共同印发了《“十三五”卫生与健康科技创新专项规划》,提出在医疗器械研发方面,重点发展医学影像设备、医用机器人、新型植入装置、新型生物医用材料、体外诊断技术与产品、家庭医疗检测和健康装备、可穿戴设备、中医医疗器械、基层适宜的诊疗设备、移动医疗等产品。
(6)《“十三五”医疗器械科技创新专项规划》
2017年5月26日,国家科技部办公厅印发了《“十三五”医疗器械科技创新专项规划》,提出在生物医用材料领域,以“组织替代、功能修复、生物调控”为方向,围绕组织器官修复、功能替代、降解调控等难点问题,重点开展生物材料的细胞组织相互作用机制、不同尺度特别是纳米尺度与不同物理因子的生物学效应等基础研究,加快发展生物医用材料表面改性、生物医用材料基因组、植入材料及组织工程支架的个性化3D打印等新技术,促进组织工程与再生医学的临床应用。

【版权提示】观研报告网倡导尊重与保护知识产权。未经许可,任何人不得复制、转载、或以其他方式使用本网站的内容。如发现本站文章存在版权问题,烦请提供版权疑问、身份证明、版权证明、联系方式等发邮件至kf@chinabaogao.com,我们将及时沟通与处理。