1美国FDA新规
美国食品药品监督管理局(FDA)于2016年5月首次电子香烟和其他电子尼古丁输送系统(ENDS)分类为烟草制品进行管制,但不包括那些作为药物、药物装置或组合产品销售(例如作为治疗产品来帮助人们戒烟)的电子烟产品。
2016年8月8日起实行新规,对所有烟草制品实施监管,具体包括电子烟、烟油、烟斗、水烟、雪茄及其他新型烟草制品。
2017年5月,FDA将各规定的截止期限推迟了3个月。在2018年11月8日后市场上未进行上市预申请的产品将禁止销售。
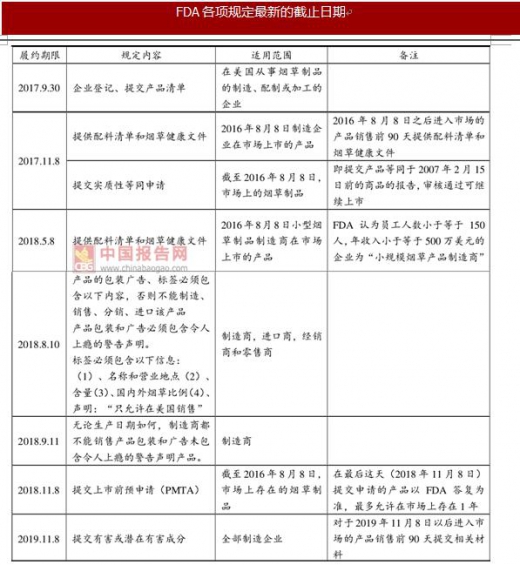
FDA根据《烟草控制法》和《食品、药物和化妆品法案》中规定的法律,对电子烟的销售、广告、促销、分销、制造、进口、包装和标签等制定了相关规定。

然而,对于有治疗目的销售的产品(例如作为帮助人戒烟的产品销售)由FDA通过药物评估和研究中心(CDER)进行监管。FDA于2017年1月发布了“烟草制品或者衍生品作为药品、器械或组合产品的说明,有关‘预定用途’的修订”,描述制造或衍生自用于人类消费的烟草的产品将作为烟草制品,药物,装置或联邦食品,药物和化妆品法案(FD&C法案)的组合产品。
此举旨在向受监管行业提供指导,并帮助避免消费者的混淆。根据“药物”和“装置”的法定定义(FD&C法案的第201(g)和(h)条),最终规定,在两种情况下,由烟草制成或衍生并用于人类消费的产品被视为药物、器械或其组合产品。

FDA还对尚未上市的烟草产品进行审查,以防烟草商发表误导性的声明。同时,还对烟草制品的成分进行评估、对生产过程进行审查并对烟草制品的潜在风险进行咨询并发出警示。
2欧盟TPD监管政策
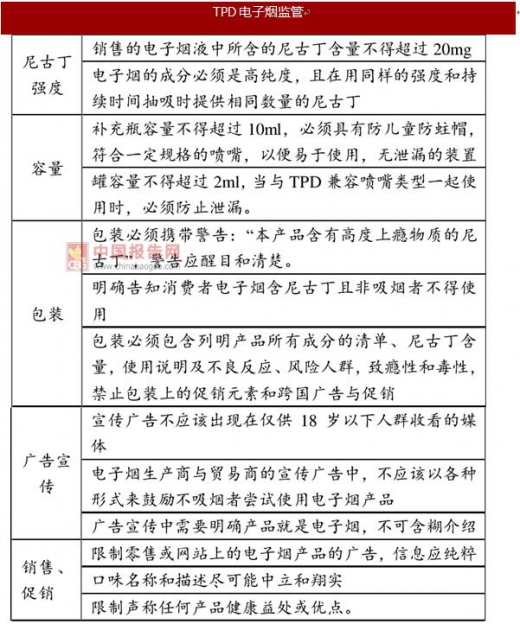
欧盟从2016年5月20日起全面实施新修订的《烟草产品指令》(TPD,TobaccoProductsDirective)对电子烟和其他相关的电子尼古丁/非尼古丁输送系统进行覆盖和监管,包括规定电子的尼古丁强度、包装和标签、补充容器尺寸、油罐容量、促销条例等。TPD指令旨在提高欧盟市场上烟草和相关产品的功能,同时提高欧洲公民健康的保护水平。该协议甚至超越了欧盟的边界,挪威和瑞士也采用欧盟TPD对电子烟进行监管。
欧盟所有国家必须以与烟草相同的方式对电子烟相关的产品进行管制,类似于美国的认定法。每个欧盟成员国可以进一步限制,但都必须遵守欧盟TPD的规则,如销售的电子烟液瓶容量不得超过10ml,烟油中尼古丁含量不得超过20mg/ml。
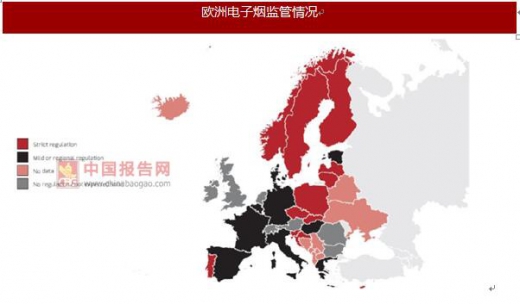
在欧洲,东欧和北欧国家有着最严厉的监管制度,将电子烟等同于直接吸入的可燃产品,电子烟被禁止使用。
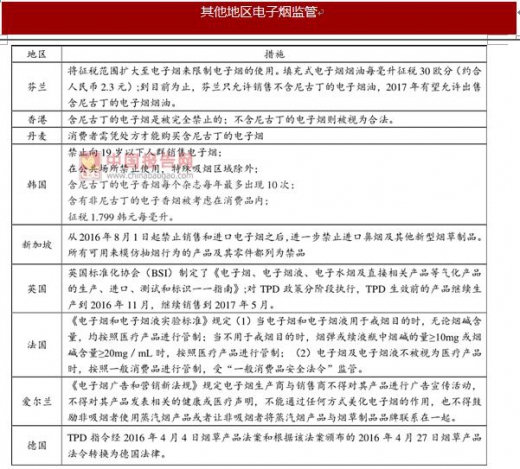
除去以上代表性国家,还有很多其他国家也出台部分电子烟的监管措施。包括欧盟部分成员国,在TPD监管基础之上制订了符合本国国情的电子烟监管政策。

【版权提示】观研报告网倡导尊重与保护知识产权。未经许可,任何人不得复制、转载、或以其他方式使用本网站的内容。如发现本站文章存在版权问题,烦请提供版权疑问、身份证明、版权证明、联系方式等发邮件至kf@chinabaogao.com,我们将及时沟通与处理。









