体外诊断行业行政主管部门为国家食品药品监督管理总局(CFDA),并归属其下设的医疗器械注册管理司和医疗器械监管司具体管理。医疗器械注册管理司的主要职能是严格依照法律法规规定的条件和程序办理第三类、进口医疗器械产品注册并承担相应责任,优化注册管理流程,组织实施分类管理,监督实施医疗器械质量管理规范。医疗器械监管司的主要职能是掌握分析医疗器械安全形势、存在的问题,并提出完善制度机制和改进工作的建议,督促下级行政机关严格依法实施行政许可、履行监督管理责任,及时发现、纠正违法和不当行为。组织开展医疗器械不良事件监测、再评价。
另外,卫计委临床检验中心也履行部分行业监督职责,主要包括:制定临床检验技术标准及管理规范;负责全国临床检验的质量管理、技术指导、临床检验仪器的质量评价、参考方法的建立、校准实验室的建立、临床检验专业人员的技术培训等。卫计委临床检验中心每年均组织临床检验室间质量评价工作,对各医疗机构检验科的检验结果质量和使用的诊断试剂进行监测和评价。
体外诊断行业的自律组织为中国医疗器械行业协会体外诊断系统专业委员会(简称“IVD专委会”)。中国医疗器械行业协会(CAMDI)成立于1991年,是从事医疗器械研发、生产、经营、投资、产品检测、认证咨询及教育培训的有关单位或个人,在自愿的基础上,联合组成的全国性、行业性、非营利性社会组织,具有社会团体法人资格,接受业务主管单位国务院国有资产监督管理委员会和社团登记管理机关民政部的业务指导和监督管理。其下属的IVD专委会主要负责体外诊断行业市场研究、参与制定相关行业标准和政策法规、对会员企业的公众服务、行业自律管理以及代表会员企业向政府部门提出产业发展建议等。
2、行业管理体制
医疗器械行业关乎人的生命健康安全,产业的监管体制较为严格,在产品注册、生产以及流通等环节均设立有严格管理制度。具体如下:
(1)分类管理制度

(2)医疗器械产品注册与备案
参考观研天下发布《2018-2023年中国体外诊断市场竞争现状分析与投资商机分析预测报告》
《医疗器械监督管理条例》(国务院令第650号)第八条规定,国家对医疗器械实行产品备案与注册管理。生产第一类医疗器械产品,需由备案人向所在地设区的市级人民政府食品药品监督管理部门提交备案资料,对予以备案的医疗器械,食品药品监督管理部门应当按照相关要求的格式制作备案凭证。生产第二类医疗器械产品,注册申请人应当向所在地省、自治区、直辖市人民政府食品药品监督管理部门提交注册申请资料,经审查、批准后发给医疗器械注册证。生产第三类医疗器械产品,注册申请人应当向国务院食品药品监督管理部门提交注册申请资料,经审查、批准后发给医疗器械注册证。
CFDA注册程序如下:
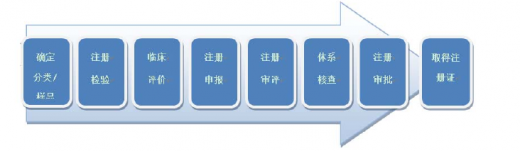
(3)生产及经营企业备案和许可证制度
医疗器械生产及经营企业在取得医疗器械产品生产及经营注册证书后,方可生产及经营医疗器械。开办第一类医疗器械生产及经营的企业,应当向省、自治区、直辖市食品药品监督管理部门备案;开办第二类、第三类医疗器械生产及经营的企业,应当经省、自治区、直辖市食品药品监督管理部门审查批准,并发给《医疗器械生产企业许可证》、《医疗器械经营企业许可证》。无《医疗器械经营企业许可证》的,工商行政管理部门不得发给营业执照。《医疗器械生产企业许可证》、《医疗器械经营企业许可证》有效期5年,有效期届满应当重新审查发证。
(4)出口销售证书以及认证
国家食品药品监督管理局于2004年2月颁布《关于出具医疗器械产品出口销售证明书的管理规定》(国食药监械[2004]34号),规定医疗器械产品出口销售必须取得医疗器械产品出口销售证明书。
此外,对于出口到国外的医疗器械产品,还必须满足进口国当地的法律法规以及认证规范,如ISO13485认证、欧盟CE认证、美国FDA认证等。
以体外诊断产品CE认证为例,其流程如下:
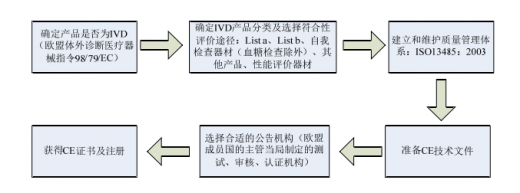
(5)医疗器械行业标准制度
为了加强医疗器械标准工作,保证医疗器械的安全、有效,国家药品监督管理局制定了《医疗器械标准管理办法》(试行),将医疗器械标准分为国家标准、行业标准和注册产品标准,医疗器械的研制、生产、经营和使用应符合相应的国家标准、行业标准或注册产品标准。
国家标准或行业标准是指需要在全国范围内统一技术要求的标准。医疗器械国家标准和行业标准由国家设立的各医疗器械专业标准化技术委员会或国务院药品监督管理部门设立的医疗器械标准化技术委员会组织制定和审核。
注册产品标准是指由制造商制定,应能保证产品安全有效,并在产品申请注册时,经注册产品标准应执行国家标准、行业标准和有关法律、法规的要求,并按国务院药品监督管理部门公布的《医疗器械注册产品标准编写规范》的要求起草。设区的市级以上药品监督管理部门依据国家标准和行业标准相关要求复核的产品标准。

【版权提示】观研报告网倡导尊重与保护知识产权。未经许可,任何人不得复制、转载、或以其他方式使用本网站的内容。如发现本站文章存在版权问题,烦请提供版权疑问、身份证明、版权证明、联系方式等发邮件至kf@chinabaogao.com,我们将及时沟通与处理。