医药
商务部、公安部和卫生健康委发布关于展览活动新冠肺炎疫情常态化防控工作的指导意见
依据《中华人民共和国传染病防治法》、《突发公共卫生事件应急条例》等法律法规,贯彻“安全第一、预防为主”的方针,依法科学开展展览活动新冠肺炎疫情常态化防控工作,充分发挥展览业在扩大开放、增加就业、稳住外贸外资基本盘、拉动消费等方面的重要作用,扎实做好“六稳”工作,全面落实“六保”任务,努力克服新冠肺炎疫情带来的不利影响,增强展览业防控和应变能力,确保防控常态化条件下各项展览活动科学稳妥、安全有序开展,推动经济社会持续向好发展。
国家卫生健康委发布关于允许医学专业高校毕业生免试申请乡村医生执业注册的意见(附解读)
允许不具备执业医师资格或者执业助理医师资格的人员申请乡村医生执业注册的盛自治区,应当于2020年7月31日前按照本意见要求,修订关于乡村医生执业注册的管理办法,允许具有全日制大专以上学历的临床医学、中医学类、中西医结合类等相关专业应届毕业生(含尚在择业期内未落实工作单位的毕业生)免试申请乡村医生执业注册。
国家药监局发布关于实施2020年版《中华人民共和国药典》有关事宜的公告
药品上市许可持有人、生产企业和药品注册申请人应积极做好执行本版《中国药典》的准备工作,对在《中国药典》执行过程中发现的问题及时向国家药典委员会报告,同时应持续研究完善药品质量标准,不断提高药品质量控制水平。
国务院应对疫情联防联控机制综合组发布《关于进一步加快提高医疗机构新冠病毒核酸检测能力的通知》(附解读)
及时开展核酸检测,是落实“四早”要求的关键措施,也是做好精准防控的基础前提。党中央、国务院高度重视新冠病毒核酸检测工作,已经多次对提升检测能力、扩大检测范围作出重要部署。各地和医疗机构要将提高核酸检测能力作为“外防输入、内防反弹”的基础性工作,加强核酸检测工作的规范管理,强化核酸检测能力储备,尽快提高检测能力,避免局部疫情出现甚至暴发时,医疗资源挤兑导致检测能力严重滞后,给疫情防控和群众健康带来不利影响。
国家中医药管理局办公室关于进一步强化中医医疗机构新冠肺炎疫情防控工作的通知
当前全国新冠肺炎疫情形势总体稳定,但近期北京市发生新冠肺炎聚集性疫情,全国多个省(区、市)出现北京确诊病例的关联病例。为指导各地中医医疗机构进一步强化新冠肺炎防控措施,巩固来之不易的防控成果,坚决防止因局部防控不力造成疫情反弹,现就有关工作通知如下:
卫生健康委发布关于做好离京人员新冠肺炎健康管理服务工作的通知(附解读 )
近日,北京市发生新冠肺炎聚集性疫情,并在多省引发相关病例,防范疫情扩散形势严峻。为指导各地做好离京人员健康管理服务工作,坚决遏制疫情传播和扩散,统筹疫情防控和正常生产生活秩序恢复,现将有关事项通知如下。
国家医疗保障局办公室关于印发医疗保障疾病诊断相关分组(CHS-DRG)细分组方案(1.0版)的通知
按照疾病诊断相关分组(DRG)付费国家试点工作安排,为落实试点工作“三步走”目标,指导各地规范DRG分组工作,我局组织制定了《医疗保障疾病诊断相关分组(CHS-DRG)细分组方案(1.0版)》(以下简称“CHS-DRG细分组”),现印发给你们,并就有关事项通知如下。
国家医保局、财政部、国家税务总局发布关于做好2020年城乡居民基本医疗保障工作的通知(附解读)
为进一步贯彻落实党的十九大关于“完善统一的城乡居民基本医疗保险制度和大病保险制度”的决策部署,落实2020年《政府工作报告》任务要求,做好城乡居民基本医疗保障工作,现就有关工作通知如下:
国家医疗保障局办公室关于配合做好进一步提升新冠病毒检测能力有关工作的通知
为贯彻落实中央应对疫情工作领导小组会议部署和《国务院应对新冠肺炎疫情联防联控机制关于做好新冠肺炎疫情常态化防控工作的指导意见》,进一步提升新冠病毒检测能力,有序引导降低偏高的检测费用,支持实现“应检尽检、愿检尽检”,助力常态化防控和复工复产复学复市,现就做好新冠病毒检测的挂网采购、价格管理和医保支付工作通知如下。
财政部办公厅关于2020年抗疫特别国债(二期)发行工作有关事宜的通知
2018-2020年记账式国债承销团成员,中央国债登记结算有限责任公司、中国证券登记结算有限责任公司、中国外汇交易中心、上海证券交易所、深圳证券交易所:
国家药监局综合司关于进一步做好案件查办工作有关事项的通知
为深入贯彻落实药品安全“四个最严”的要求,进一步推进案件查办工作,严厉打击违法违规行为,切实加强药品安全监管,结合新制修订的法律法规,现就进一步做好药品、医疗器械、化妆品案件查办工作通知如下:
卫生健康委发布关于加快推进新冠病毒核酸检测的实施意见(附解读)
党中央、国务院高度重视新冠病毒核酸检测工作,中央应对新型冠状病毒感染肺炎疫情工作领导小组会议作出部署,要求着力提升检测能力,尽力扩大检测范围。加强核酸检测工作,既有利于巩固防控成果,维护群众健康,又有助于人员合理流动,推动全面复工复产复学,是“外防输入、内防反弹”的重要措施。为指导各地在常态化防控工作中做好核酸检测工作,提出如下意见:
2020年中国药品流通行业主管部门和行业监管体制、主要法律法规及政策
以企业为代表的院外市场医药流通综合服务企业,将服务下沉至基层医疗机构,有力的支持了国家对基层医疗机构的建设规划;在区域内率先引入互联网及大数据技术,大幅提高流通效率、降低流通成本。
外交部就李克强总理在全球疫苗峰会视频会议上致辞相关情况等答问
澎湃新闻记者:美国运输部3日发布声明称,为回应中国政府未能允许美承运方完全行使提供往返中国客运服务的双边权利,美方决定自6月16日起暂停中国航空公司往返美国的定期航班。中方对此有何评论?
国家卫生健康委发布关于学习贯彻习近平总书记重要指示精神进一步加强护士队伍建设的通知
习近平总书记的重要指示充分体现了党和国家对护理工作的高度重视,对广大护士的亲切关怀和殷切希望,是新时代加强护士队伍建设的基本遵循和行动指南。认真学习和贯彻落实好习近平总书记重要指示精神,对于加强护士队伍建设,发展卫生健康事业,推进健康中国建设,积极应对人口老龄化具有重大而深远的意义。
国家药监局发布关于批准注册235个医疗器械产品公告(2020年4月)
2020年4月,国家药品监督管理局共批准注册医疗器械产品235个。其中,境内第三类医疗器械产品134个,进口第三类医疗器械产品38个,进口第二类医疗器械产品62个,港澳台医疗器械产品1个(具体产品见附件)。
卫生健康委发布关于《关于进一步完善预约诊疗制度加强智慧医院建设的通知》
为进一步发挥互联网医疗服务在巩固疫情防控成果和改善医疗服务中的积极作用,持续推动预约诊疗、智慧医院、互联网诊疗和互联网医院快速健康发展,近日,国家卫生健康委印发了《关于进一步完善预约诊疗制度加强智慧医院建设的通知》,指导各地和各医院在疫情常态化防控下,进一步建立完善预约诊疗制度,加强智慧医院建设,加快建立线上线下一体化的医疗服务新模式,不断增强人民就医获得感。
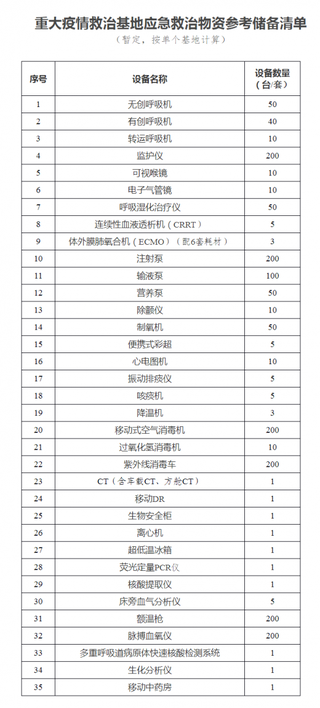
国家发展改革委、国家卫生健康委、国家中医药局发布关于公共卫生防控救治能力建设方案的通知
全面贯彻习近平总书记系列重要指示批示精神,落实党中央、国务院决策部署,聚焦新冠肺炎疫情暴露的公共卫生特别是重大疫情防控救治能力短板,调整优化医疗资源布局,提高平战结合能力,强化中西医结合,深入实施爱国卫生运动,集中力量加强能力建设,补齐短板弱项,构筑起保护人民群众健康和生命安全的有力屏障。
国家中医药管理局办公室发布关于中医病案质量控制中心建设与管理指南(试行)的通知
病案质量管理与医疗质量密切相关,是医疗质量管理的核心内容之一。为加强中医病案管理,促进中医病案质量控制中心建设与发展,持续提升医疗机构中医病案管理质量,根据《医疗质量管理办法》《医疗质量控制中心管理办法(试行)》《医疗机构病历管理规定》《中医病历书写基本规范》《电子病历应用管理规范(试行)》《中医住院病案首页数据填写质量规范(暂行)》等相关规定,制定本指南。